Вода для инъекций (WFI)
Фармацевтическая вода высшего качества для инъекционных препаратов.
WFI (Water for Injection, вода для инъекций) — фармацевтическая вода высшего класса чистоты для производства инъекционных лекарственных препаратов, парентерального питания и офтальмологических растворов. Регламентируется тремя основными фармакопеями мира: USP (United States Pharmacopeia, США), EP (European Pharmacopoeia, Европа), JP (Japanese Pharmacopoeia, Япония).
Почему WFI — самая строгая категория:
- Прямой контакт с кровью: инъекционные препараты минуют естественные барьеры организма (кожа, ЖКТ) → любые загрязнения (бактерии, эндотоксины, частицы) вызывают тяжёлые реакции — пирогенный шок, сепсис, тромбозы
- Эндотоксиновая опасность: мёртвые бактерии выделяют эндотоксины (липополисахариды клеточной стенки грамотрицательных бактерий) → при концентрации > 0.25 EU/мл вызывают лихорадку, гипотензию, полиорганную недостаточность; эндотоксины термостабильны — выдерживают автоклавирование 121°C, обычная стерилизация не помогает
- Нулевая толерантность к загрязнениям: WFI используется для разведения антибиотиков, противоопухолевых препаратов, вакцин — концентрация активной субстанции 10⁻⁶-10⁻⁹ г/мл, любая примесь (металлы, органика) искажает дозировку и вызывает побочные эффекты
- Регуляторный контроль: производство WFI требует сертификации GMP (Good Manufacturing Practice, надлежащая производственная практика), ежегодных аудитов регуляторов (FDA, EMA, Росздравнадзор) → нарушения приводят к остановке производства и отзыву партий препаратов стоимостью $10-50 млн
Ультрафильтрация для WFI

Требования качества WFI по фармакопеям
Три основные фармакопеи (USP, EP, JP) предъявляют практически идентичные требования к WFI, с небольшими различиями в методах контроля.
Таблица параметров WFI:
| Параметр | USP (США) | EP (Европа) | JP (Япония) | Метод контроля | Критичность |
|---|---|---|---|---|---|
| Электропроводность при 25°C | < 1.3 мкСм/см | < 1.1 мкСм/см | < 1.3 мкСм/см | Онлайн кондуктометр | Превышение → остановка производства |
| TOC (Total Organic Carbon) | < 500 ppb | < 500 ppb | < 500 ppb | УФ окисление + CO₂ детектор | > 500 ppb → забракована партия |
| Бактериальные эндотоксины | < 0.25 EU/мл | < 0.25 EU/мл | < 0.25 EU/мл | LAL-тест (Limulus) | > 0.25 EU → пирогенная реакция |
| Микробиологическая чистота | < 10 CFU/100 мл | < 10 CFU/100 мл | < 10 CFU/100 мл | Посев на TSA + SDA, 7 дней | > 10 CFU → контаминация |
| Нитраты (NO₃⁻) | < 0.2 мг/л | < 0.2 мг/л | < 0.2 мг/л | Ионная хроматография | Метгемоглобинемия |
| Тяжёлые металлы (Pb, Cd, Hg) | < 0.1 мг/л | < 0.1 мг/л | < 0.1 мг/л | ICP-MS | Токсичность, искажение анализов |
Ключевые отличия EP (изменение 2017 года): До 2017 года EP требовала обязательную дистилляцию для WFI. С апреля 2017 EP Monograph 0169 допускает мембранные методы (RO + EDI + UF) при условии валидации по удалению эндотоксинов (Log Reduction Value > 3, т.е. снижение в 1000 раз). USP допускает мембраны с 2008 года, JP — с 2016.
Почему эндотоксины — главная проблема: Эндотоксины (ЛПС — липополисахариды) имеют молекулярную массу 10-1000 кДа, размер 5-20 нм. Они проходят через обычные фильтры и мембраны RO (селективность RO по солям 99%, по эндотоксинам — только 90-95%). Единственные эффективные методы удаления:
- Дистилляция: эндотоксины не испаряются, остаются в кубе → rejection > 99.9%
- Ультрафильтрация 0.001-0.003 мкм (1-3 нм MWCO): механическое задержание молекул > 10 кДа
- Высокотемпературная обработка > 250°C 30 мин: пиролиз (разрушение) эндотоксинов, но невозможна для готовой воды
- Адсорбция на Charge-Modified фильтрах: положительно заряженные мембраны притягивают отрицательно заряженные ЛПС
Методы получения WFI: дистилляция vs мембраны
1. Многоколонная дистилляция (классический метод, gold standard):
Схема: Purified Water (исходная) → многоколонный дистиллятор (3-6 эффектов) → WFI
- Принцип: испарение воды при 100-105°C, конденсация чистого пара; эндотоксины, бактерии, соли, органика остаются в кубовом остатке
- Производительность: 500-10 000 л/час на установку
- Эффективность: rejection эндотоксинов > 99.9%, бактерий 100%
- Энергозатраты: 50-80 кВт·ч/м³ (нагрев + охлаждение пара)
- CAPEX: 1.5-3.5 млн руб за установку 1000 л/час
- OPEX: 400-800 руб/м³ (электроэнергия, обслуживание, замена прокладок)
Преимущества дистилляции:
- Абсолютная надёжность удаления эндотоксинов (> 99.9%)
- Признаётся всеми фармакопеями без ограничений с 1940-х годов
- Не требует сложной валидации (IQ/OQ/PQ достаточно)
- Низкие требования к исходной воде (достаточно Purified Water с проводимостью < 5 мкСм/см)
Недостатки:
- Высокие энергозатраты 50-80 кВт·ч/м³ → OPEX 400-800 руб/м³
- Медленный пуск (прогрев 1-2 часа до стационарного режима)
- Накипеобразование в кубе при жёсткости исходной воды > 50 мг/л CaCO₃ → еженедельная CIP-мойка лимонной кислотой
- Потери воды 15-30% с кубовым остатком
2. Мембранные методы (разрешены EP с 2017, USP с 2008):
Схема: Purified Water → 2-pass RO → EDI → UF 0.001-0.003 мкм (депирогенизирующая) → УФ 254 нм → WFI
- Принцип: RO + EDI удаляют соли, органику, бактерии; финальная ультрафильтрация 1-3 нм (MWCO 10-30 кДа) задерживает эндотоксины > 10 кДа; УФ 254 нм инактивирует бактерии
- Производительность: 500-20 000 л/час (масштабируется легко)
- Эффективность: rejection эндотоксинов 99.5-99.8% (LRV = 2.5-3), бактерий > 99.99%
- Энергозатраты: 5-12 кВт·ч/м³ (только насосы, без нагрева)
- CAPEX: 3-8 млн руб за установку 1000 л/час (дороже дистилляции из-за сложности)
- OPEX: 150-350 руб/м³ (электроэнергия, замена мембран UF раз в 12-24 месяца)
Преимущества мембран:
- Низкие энергозатраты 5-12 кВт·ч/м³ → OPEX на 50-65% ниже дистилляции
- Мгновенный пуск (3-5 минут до рабочего режима)
- Компактность (занимают в 2-3 раза меньше места)
- Нет накипеобразования, минимальная CIP-мойка (раз в 3-6 месяцев)
Недостатки:
- Требуется сложная валидация IQ/OQ/PQ + ежегодная ревалидация на удаление эндотоксинов (LAL-тест, spiking studies)
- Высокие требования к исходной воде (Purified Water с проводимостью < 1.3 мкСм/см, TOC < 500 ppb)
- Риск проскока эндотоксинов при прорыве UF-мембраны → требуется онлайн-мониторинг LAL-теста (дорого, $50-100k)
- Срок службы UF-мембран 12-24 месяца (замена $20-50k на установку 1000 л/час)
Когда выбирать дистилляцию:
- Производство < 2 000 л/час (CAPEX мембран не окупается)
- Исходная вода низкого качества (скважина, поверхностный источник)
- Консервативная позиция регуляторов (Росздравнадзор до 2020 предпочитал дистилляцию)
Когда выбирать мембраны:
- Производство > 3 000 л/час (экономия OPEX $30-80k/год)
- Ограничения по энергомощности (мембраны в 5-7 раз экономичнее)
- Дефицит места (мембраны компактнее в 2-3 раза)
- Частые пуски/остановки (мембраны готовы за 3 минуты, дистилляция — за 1-2 часа)
Мембранная система RO + EDI
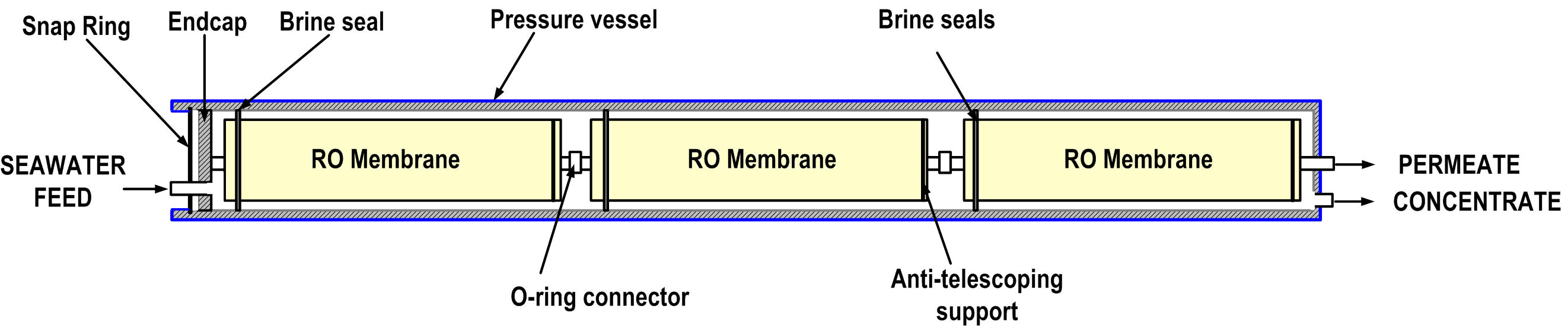
Хранение и распределение WFI
WFI — нестабильная система. Без специальных мер рост бактерий начинается через 4-8 часов, эндотоксины накапливаются через 12-24 часа.
Два подхода к хранению:
1. Горячее хранение (Hot Storage, предпочтительно):
- Температура хранения > 70°C (обычно 75-85°C)
- Принцип: при > 70°C большинство бактерий погибают за 2-4 часа, споры не прорастают, биоплёнка не образуется
- Распределение в замкнутой петле при > 80°C (обычно 80-85°C) → постоянная циркуляция со скоростью 1-2 м/с
- Материалы: только нержавейка 316L с электрополировкой (Ra < 0.5 мкм) или специальные полимеры (PVDF, PFA для температур до 120°C)
- CAPEX: +30-50% к стоимости системы (нагреватели, теплоизоляция, специальная арматура)
- OPEX: +150-250 руб/м³ на электроэнергию для поддержания температуры
Преимущества:
- Микробиологическая стабильность без химической санитизации
- Не требуется частая CIP-мойка (раз в 3-6 месяцев vs раз в 1-2 недели для холодного хранения)
- Проще валидация (температура > 70°C сама по себе метод стерилизации)
Недостатки:
- Высокие энергозатраты (+150-250 руб/м³)
- Опасность ожогов персонала при обслуживании
- Термические расширения труб → требуются компенсаторы
- Ограничения по полимерным материалам (большинство выдерживают только до 60-80°C)
2. Холодное хранение (Cold Storage):
- Температура хранения < 4°C (обычно 2-4°C, иногда до 10°C с частой санитизацией)
- Принцип: низкая температура замедляет рост бактерий (цикл деления 48-72 часа vs 2-4 часа при 25°C)
- Требуется периодическая химическая/термическая санитизация: озон 0.5-1.5 мг/л 20-30 мин раз в 1-3 дня, или термическая санитизация > 80°C 1 час раз в неделю, или паровая стерилизация 121°C 30 мин раз в 2 недели
- Материалы: нержавейка 316L, PVDF, PFA (менее критично, чем для горячего хранения)
- CAPEX: ниже на 20-30% vs горячего хранения (холодильные установки дешевле нагревателей)
- OPEX: +50-100 руб/м³ на охлаждение + санитизацию
Преимущества:
- Ниже CAPEX и энергозатраты
- Безопаснее для персонала
- Подходят стандартные материалы
Недостатки:
- Требуется частая санитизация (раз в 1-7 дней)
- Риск контаминации между циклами санитизации
- Сложнее валидация (нужно доказать эффективность санитизации)
Критичные ошибки распределения:
Dead Legs (тупиковые отводы): Фармакопеи (USP, EP) требуют dead legs < 6D (6 диаметров трубы) или < 3D для критичных участков. Dead leg 1 метр на трубе Ø 50 мм (DN50) = 20D → застой воды > 5 минут → рост бактерий через 12-24 часа → эндотоксины > 0.25 EU/мл через 48 часов. Фармзавод в Индии (2018): dead legs 2 метра → контаминация WFI через 3 недели → отзыв 15 партий инъекционных препаратов = убыток $4.5 млн.
Низкая скорость циркуляции: Скорость < 0.8 м/с → ламинарный режим → осаждение частиц, рост биоплёнки на стенках. Биоплёнка толщиной 10 мкм выделяет эндотоксины 0.5-2 EU/мл через 7-10 дней. Фармзавод в Германии (2019): снизили скорость с 1.5 до 0.6 м/с для экономии → через 2 месяца эндотоксины 0.8 EU/мл → остановка производства на 4 недели = убыток €12 млн.
Материалы с шероховатостью > 0.5 мкм: Шероховатость Ra > 0.5 мкм создаёт микрониши для бактерий. Стандартная нержавейка 316L (Ra 0.8-1.2 мкм) → биоплёнка через 2-3 недели. Требуется электрополировка до Ra < 0.5 мкм (зеркальная поверхность).
Недооценка качества Purified Water: Если исходная Purified Water содержит > 50 CFU/мл бактерий или > 2 EU/мл эндотоксинов, даже дистилляция не гарантирует WFI качества (риск уноса капель кубовой жидкости с паром, прорыв брызгоуловителей). Фармзавод в России (2020): Purified Water с 120 CFU/мл → дистиллятор давал WFI с 3-8 CFU/100 мл (норма < 10, но нестабильно) → модернизация системы Purified Water обошлась в 8 млн руб.
Неправильный выбор метода: Установка мембранной системы при производстве < 1000 л/час → CAPEX не окупается (дистилляция на 30-40% дешевле). Фармзавод в Беларуси (2021): мембранная система 500 л/час за 6.5 млн руб вместо дистиллятора за 2.8 млн руб → переплата 3.7 млн, окупаемость разницы OPEX > 12 лет.
Отсутствие онлайн-мониторинга эндотоксинов: Мембранные системы требуют онлайн-контроля эндотоксинов (LAL-тест или BET — Bacterial Endotoxin Test). Стандартный офлайн-контроль раз в смену → отклонения обнаруживаются через 8-12 часов, за это время производится 5-15 м³ некондиционной WFI → браковка готовых препаратов. Онлайн-система BET: CAPEX $50-100k, окупаемость 1-2 инцидента.
Стагнация в нерабочее время: Остановка циркуляции WFI > 4 часов → рост бактерий. Фармзавод в Польше (2019): отключали циркуляцию на выходные (48 часов) → в понедельник CFU 45-180/100 мл (норма < 10) → слив и санитизация системы 6-8 часов + брак первых 2 м³ WFI = убыток €5-8k/месяц. Решение: 24/7 циркуляция или автоматическая санитизация перед пуском.
Проектирование WFI систем требует экспертизы в фармацевтической водоподготовке:
- Выбор метода (дистилляция vs мембраны) под производительность, энергомощность, требования регуляторов
- Расчёт системы хранения и распределения (горячая/холодная петля, скорости, dead legs)
- Подбор материалов (нержавейка 316L с электрополировкой, PVDF, PFA)
- Проектирование CIP-систем (Clean-In-Place) и санитизации
- Разработка онлайн-мониторинга (проводимость, TOC, температура, эндотоксины)
- Валидация IQ/OQ/PQ по требованиям GMP
- Подготовка документации для аудитов FDA, EMA, Росздравнадзора
Инженеры ВАКО имеют опыт проектирования WFI систем для фармпроизводств:
- Дистилляционные установки 500-10 000 л/час (многоколонные, с утилизацией тепла)
- Мембранные системы 500-20 000 л/час (RO + EDI + депирогенизирующая UF)
- Горячие/холодные петли распределения с валидацией
- Системы онлайн-мониторинга качества
CAPEX WFI системы (1000 л/час):
- Дистилляция: 2.5-4 млн руб (генерация) + 1.5-3 млн руб (хранение/распределение) = 4-7 млн руб
- Мембраны: 4-8 млн руб (генерация) + 2-4 млн руб (хранение/распределение) = 6-12 млн руб
OPEX:
- Дистилляция: 400-800 руб/м³
- Мембраны: 150-350 руб/м³
Обсудить проект: +7 (989) 122-83-08 или info@vaco-eng.ru
Связанные материалы
Нужна консультация по водоподготовке?
Рассчитаем технологию, подберём оборудование и ответим на вопросы. Ответим в течение 24 часов.