Основы ионного обмена
Введение
 Ионный обмен — это мощная химическая технология, малоизвестная широкой публике. Данная статья объясняет суть ионного обмена для тех, кто не является специалистом в химии.
Ионный обмен — это мощная химическая технология, малоизвестная широкой публике. Данная статья объясняет суть ионного обмена для тех, кто не является специалистом в химии.
Когда знакомые спрашивают меня о моей профессиональной деятельности, я отвечаю: «ионный обмен». Большинство из них понятия не имеют, что это такое. При этом в Западной Европе у многих моих знакомых дома есть одно-два устройства, работающих на принципе ионного обмена. Поэтому я задаю встречный вопрос: «Как вы думаете, зачем вы засыпаете соль в посудомоечную машину?» Ответить могут единицы — если вы тоже не знаете, ниже вы найдёте ответ.
Вода
Вода кажется простым веществом: она состоит из молекул воды (формула H2O). Однако вы знаете, что эта кажущаяся простота на самом деле сложнее: иначе производители бутилированной воды не уделяли бы столько внимания её минерализации.
Все природные воды содержат посторонние вещества, обычно в небольших количествах. Вода в реке, в колодце или из крана у вас дома — это не просто H2O, она содержит:
- Твёрдые нерастворимые вещества — песок, растительные остатки и т.п. Их можно отфильтровать механическим путём.
- Растворённые вещества, которые чаще всего невидимы и не могут быть удалены фильтрацией. Они могут быть неорганическими или органическими, ионизированными (электрически заряженными) или неионизированными.
Растворимые неионизированные вещества присутствуют в воде в виде молекул различных размеров и формул, например:
- Диоксид углерода — небольшая молекула с простой формулой: CO2.
- Сахар — более крупная молекула со сложной формулой C12H22O11. Сахара не удаляются ионным обменом.
Если вам нужно удалить из воды посторонние вещества, то ионизированные вещества можно удалить методом ионного обмена.
Ионы
Растворимые ионизированные вещества присутствуют в воде в виде ионов — электрически заряженных атомов или молекул. Положительно заряженные ионы называются катионами, отрицательно заряженные — анионами. Поскольку вода электрически нейтральна (иначе вы получили бы удар током, опустив руку в воду), число положительных зарядов равно числу отрицательных.
Ионы могут иметь один или несколько зарядов (обычно от 1 до 3). Ионы могут состоять из одного атома (одноатомные ионы) или из нескольких атомов, прочно связанных между собой, подобно молекулам (многоатомные ионы).
Примеры:
- Одновалентный одноатомный катион: ион натрия Na+
- Двухвалентный одноатомный катион: ион кальция Ca++
- Одновалентный многоатомный катион: ион аммония NH4+
- Одновалентный одноатомный анион: ион хлора Cl−
- Одновалентный многоатомный анион: нитрат-ион NO3−
- Двухвалентный многоатомный анион: карбонат-ион CO3=
- Ещё один двухвалентный многоатомный анион: хромат-ион CrO4=
- Трёхвалентный одноатомный катион алюминия Al+++ существует только в очень кислых растворах, но не в обычной воде.
Ионы свободно перемещаются в воде, они не зафиксированы и не связаны с ионами противоположного знака. Только сумма зарядов всех катионов и всех анионов остаётся постоянной. На рисунке 1 показано схематическое изображение ионов в воде.
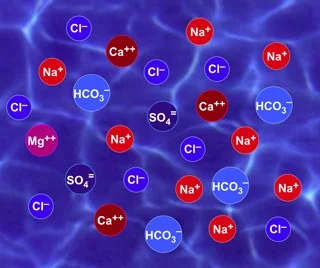
Соли — это кристаллические вещества, содержащие определённое соотношение катионов и анионов. Например, поваренная соль содержит одинаковое число катионов натрия (Na+) и анионов хлора (Cl−). Её формула — NaCl. При растворении соли в воде её катионы и анионы диссоциируюти свободно перемещаются, как показано на рисунке 1.
Растворённые ионы окружены молекулами воды — они гидратированы. Они непрочно связаны с молекулами воды: катионы притягиваются к атому кислорода, анионы — к атомам водорода молекулы воды (рисунок 2).
Ионное соединение, растворённое в воде
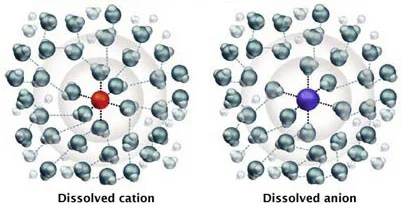
Сульфат магния — соль с одинаковым числом катионов магния (с двойным зарядом: Mg++) и сульфат-анионов (также с двойным зарядом: SO4=), поэтому формула — MgSO4.
Хлорид кальция состоит из ионов кальция (с двумя зарядами: Ca++) и ионов хлора (с одним зарядом: Cl−). Для компенсации каждого катиона кальция нужны два аниона хлора. Поэтому формула хлорида кальция — CaCl2.
Аналогично, в карбонате натрия присутствуют катионы натрия Na+ и карбонат-анионы CO3=, поэтому на каждый карбонат-ион приходится два иона натрия, и формула — Na2CO3.
При длительном кипячении и выпаривании воды остаётся сухой остаток, состоящий из солей и, возможно, других веществ, таких как кремнезём и органические соединения. Только в морской воде сухой остаток значителен: 35–40 г на литр воды. В речной или водопроводной воде сухой остаток обычно очень низкий: от 50 до 500 мг/л. Сухой остаток также называется общим содержанием растворённых веществили по-английски TDS (Total Dissolved Solids).
Подробнее об анализе воды и единицах измерения концентрации, используемых в ионном обмене. Важно понимать, что в ионном обмене значение имеет не масса (г) и не молярность (моль), а «эквивалентная масса»:
1 экв = 1 моль / валентность
Один моль натрия (Na+) содержит 23 г металла. Поскольку натрий одновалентен, один эквивалент Na+ также соответствует 23 г. Но один моль никеля (Ni++) содержит 58,7 г металла, и один эквивалент Ni++ составляет лишь 29,35 г.
Ионный обмен
Примеси в воде
Примеси? Как мы видели, вода содержит небольшие количества посторонних веществ. Во многих случаях эти вещества не создают проблем и не должны считаться примесями. Питьевая вода с некоторым содержанием солей гораздо полезнее для здоровья, чем ультрачистая вода. Однако для специальных применений эти посторонние вещества рассматриваются как примесии должны быть удалены из воды.
Нерастворимые вещества (песок и т.п.) можно удалить фильтрацией. Существует множество различных технологий фильтрации, вплоть до ультрафильтрации, которая может удалять субмикронные частицы. Для удаления растворённых веществ необходимы другие методы.
Растворённые ионизированные вещества можно удалить методом ионного обмена.
Ионообменные смолы
Это очень маленькие пластиковые гранулы диаметром около 0,6 мм. Гранулы пористые и содержат внутри невидимую воду, измеряемую как «влажность» или «влагосодержание». Структура смолы представляет собой полимер (как и все пластики), к которому прочно присоединён фиксированный ион. Этот ион нельзя удалить или вытеснить — он является частью структуры. Для сохранения электрической нейтральности смолы каждый фиксированный ион должен быть нейтрализован противоионом(подвижным ионом). Этот противоион может входить в гранулу смолы и выходить из неё.
На рисунке 3 показана схема гранулы катионообменной смолы (катионита). Тёмные линии изображают полимерный скелет гранулы: он пористый и содержит воду. Фиксированные ионы этого катионита — сульфогруппы (SO3−), присоединённые к скелету. На рисунке подвижными ионами являются катионы натрия (Na+). Катиониты, такие как Amberjet 1000, обычно поставляются в натриевой форме.
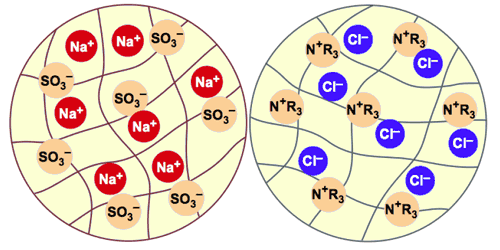
Гранула анионообменной смолы (анионита) имеет очень похожий скелет. Функциональными группами здесь являются катионы четвертичного аммония, показанные на рисунке как N+R3; более точная формула: CH2—N+(—CH3)3. Каждый ион, входящий в гранулу, должен быть заменён ионом, выходящим из неё, — для сохранения электрической нейтральности. Это и называется ионным обменом. Обмениваются только ионы одного знака. Невозможно создать смолу, которая обменивает и катионы, и анионы, поскольку фиксированные катионы внутри гранулы нейтрализовали бы фиксированные анионы, и обмен с внешней средой стал бы невозможен. Поэтому нужны отдельные катионообменные и анионообменные смолы.
Подробнее о структуре смол — на отдельной странице.
Умягчение воды
Среди веществ, растворённых в воде, очень часто встречается жёсткость. Жёсткость — это общепринятый термин для обозначения преимущественно кальция и магния, растворённых в воде. Эти ионы при определённых условиях могут выпадать в осадок и образовывать накипь, которую вы, возможно, видели в чайнике и которая может засорять трубы и повреждать водонагреватели. «Умягчение» воды — это обмен ионов жёсткости (Ca++ и Mg++) на другой катион, который не образует накипь благодаря гораздо большей растворимости, — ион натрия Na+.
Для умягчения воды берётся катионит, в котором подвижным ионом внутри гранул является натрий (Na+), и жёсткая вода пропускается через колонну, заполненную смолой в натриевой форме. Ионы жёсткости Ca++ и Mg++ переходят в гранулы смолы, и каждый из этих двухвалентных катионов замещается двумя ионами натрия, выходящими из смолы. Реакция обмена записывается так:
2 RNa + Ca++ → R2Ca + 2 Na+
Этот катионный обмен эффективен только потому, что катионит имеет более высокое сродствок ионам жёсткости, чем к натрию. Проще говоря, смола «предпочитает» кальций и магний натрию. Результатом умягчения является не полное удаление ионов жёсткости из воды, а их замена на ионы натрия. Солесодержание воды не изменилось, изменился лишь состав солей.
Очевидно, что этот обмен не безграничен: когда смола поглотит столько ионов жёсткости из исходной воды, что в ней не останется места для поглощения новых, рабочий цикл необходимо остановить. На этом этапе смола должна быть заменена на свежую или регенерирована.
Обессоливание (деминерализация)
Если заменить все катионы, растворённые в воде, на ионы H+, а все анионы — на ионы OH−, они соединятся и образуют новые молекулы воды. Для этого нужен катионит в H-форме и анионит в OH-форме. Все катионы и анионы будут обменены, и в результате произойдёт полное «исчезновение» ионных загрязнений. Реакции катионного обмена будут следующими:
2 R'H + Ca++ → R'2Ca + 2 H+
R'H + Na+ → R'Na + H+
В этих уравнениях R' обозначает катионообменную смолу.
Аналогично, анионит, изначально находящийся в OH−-форме, может удалить все анионы:
R''OH + Cl− → R''Cl + OH−
2 R''OH + SO4= → R''2SO4 + 2 OH−
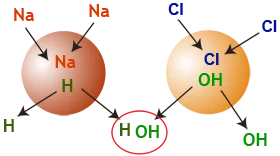
Ионы H+ и OH− немедленно соединяются и образуют воду:
H+ + OH− → HOH → H2O
Ионные загрязнения теперь находятся на двух смолах, а вода полностью обессолена. Её солесодержание снижено почти до нуля — остаются лишь несколько ионов, которые «проскочили» через колонны со смолой. Это называется проскоком ионов.
Регенерация
Когда смолы истощены, их можно вернуть в исходное состояние и начать цикл заново. Регенерация ионообменных смол — это обращение реакций обмена.
Регенерация умягчителя
 Умягчительная смола регенерируется ионами натрия (Na+), поступающими из раствора поваренной соли (NaCl). Реакция регенерации:
Умягчительная смола регенерируется ионами натрия (Na+), поступающими из раствора поваренной соли (NaCl). Реакция регенерации:
R2Ca + 2 NaCl → 2 RNa + CaCl2
Регенерация возможна только при высокой концентрации регенерирующего раствора — обычно в 1000 раз выше, чем концентрация солей в обычной воде. Например, для регенерации используется рассол с концентрацией около 10% (примерно 100 г/л).
Теперь вы понимаете, зачем засыпать соль в посудомоечную машину: соль растворяется водой и регенерирует невидимый умягчительный картридж, обычно расположенный в нижней части машины.
Регенерация обессоливающей установки
В случае обессоливания сильные кислоты, такие как соляная кислота (HCl) или серная кислота (H2SO4), полностью диссоциированы и могут поставлять ионы H+:
R'Na + HCl → R'H + NaCl
Аналогично, едкий натр NaOH может поставлять ионы OH−:
R''Cl + NaOH → R''OH + NaCl
Как видно из реакций регенерации, на этапе регенерации образуются солевые стоки. Это основной недостаток ионного обмена.
Смотрите описание полного цикла и страницу с методами прямоточной и противоточной регенерации.
Как выглядят смолы



Полная страница с многочисленными фотографиями смол под микроскопом.
Обменная ёмкость
Полная ёмкость — количество «активных групп» или «функциональных групп» в ионообменной смоле. Поскольку в одной грануле смолы миллиарды отдельных активных групп, ёмкость обычно выражается в эквивалентах на литр смолы. Один эквивалент равен 6,02×1023 активных групп (число Авогадро).
- Типичный сильнокислотный катионит имеет полную ёмкость 1,8–2,2 экв/л
- Типичный слабокислотный катионит имеет полную ёмкость 3,7–4,5 экв/л
- Типичный слабоосновный или сильноосновный анионит имеет полную ёмкость 1,1–1,4 экв/л
Рабочая ёмкость определяется как разница между количеством регенерированных центров в начале и в конце рабочего цикла. Она также измеряется в эквивалентах на литр. В работе рабочая ёмкость смолы составляет примерно половину полной ёмкости. Фактический диапазон — от 40 до 70% полной ёмкости в зависимости от условий эксплуатации. Подробнее см. на отдельной странице.
Важно: В ионном обмене важно количество ионов и их заряд (один, два или три заряда на ион), а не их масса. Поэтому во всех анализах исходной воды масса ионов должна быть пересчитана в эквиваленты.
Ограничения ионного обмена
Для эффективного ионного обмена должна существовать разница в сродстве между ионом в смоле и ионом или ионами, которые вы хотите удалить из раствора. Смола должна иметь более высокое сродство к иону в растворе по сравнению с ионом в смоле.
Технология ионного обмена — идеальный инструмент для удаления или обмена загрязнений, присутствующих в низких концентрациях. В этом случае время работы до истощения колонны со смолой может быть очень долгим — от нескольких часов до нескольких месяцев.
Однако когда концентрация загрязнений высока (несколько граммов на литр воды), циклы ионного обмена становятся чрезмерно короткими, а расход реагентов возрастает до неэкономичного уровня. В случае солоноватой воды или морской воды ионный обмен не подходит, и должны использоваться другие технологии, такие как обратный осмос или дистилляция.
Кроме того, любое загрязнение, которое не ионизировано, не может быть удалено ионным обменом. Для этого существуют другие технологии с использованием активированного угля, полимерных адсорбентов, молекулярных сит и других материалов.
Селективный ионный обмен
Благодаря различиям в сродстве к разным ионам обычные ионообменные смолы могут использоваться для селективного удаления ионов из воды. Один из наиболее очевидных примеров — умягчение.
Порядок сродства для анионитов:
SO4= > NO3− > Cl− > HCO3− > OH− > F−
Для катионитов, используемых в умягчителях:
Pb++ > Ca++ > Mg++ > Na+ > H+
Свинец (Pb) показан здесь, чтобы указать, что любой растворённый свинец будет эффективно удалён умягчительной смолой, как и многие другие (но не все) тяжёлые металлы.
Некоторые загрязнения трудно удалить обычными ионообменными смолами. Селективные смолы доступны для удаления:
- Бора
- Нитратов
- Перхлоратов
- Никеля
- Хроматов
Заключение
 Ионный обмен — это очень мощная технология для удаления примесей из воды и других растворов. Многие отрасли промышленности зависят от ионного обмена для производства чрезвычайно чистой воды. Примеры:
Ионный обмен — это очень мощная технология для удаления примесей из воды и других растворов. Многие отрасли промышленности зависят от ионного обмена для производства чрезвычайно чистой воды. Примеры:
- Атомные и тепловые электростанции
- Производство полупроводников, микросхем и дисплейных панелей
- Селективное удаление токсичных загрязнений из питьевой воды
Существует также множество применений в областях, не связанных с водоподготовкой. Перейдите к карте сайта для получения подробных страниц о применениях, процессах, свойствах смол и многом другом.
Amberjet, Amberlite и Amberpack — оригинальные торговые марки Rohm and Haas, дочерней компании Dow Chemical Company.