Детали анализа воды
Введение
Эта страница охватывает анализ воды, необходимый для применений ионного обмена. Он значительно проще, чем анализ, который вы бы использовали для оценки качества питьевой воды.
Общие характеристики исходной воды описаны на другой странице с рекомендованными пределами для определённых загрязнителей и параметров. Здесь мы фокусируемся на неорганических компонентах, растворённых в воде.
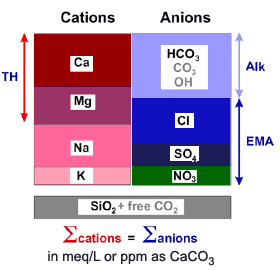
Некоторые компоненты традиционно группируются:
| Ca++ + Mg++ | = | Общая жёсткость (TH) |
| HCO3− + CO3= + OH− | = | m-Щёлочность |
| Cl− + SO4= + NO3− | = | ЭМК |
- Кальций и магний составляют Общую жёсткость (TH).
- Бикарбонат, карбонат и гидроксид составляют Общую щёлочность (m-Alk). Обычно природная вода не содержит карбонат или гидроксид.
- Хлорид, сульфат и нитрат составляют Эквивалентную минеральную кислотность(ЭМК), также называемую Солями сильных кислот (ССК).
- Когда жёсткость больше щёлочности (в мэкв/л), бикарбонатная жёсткость называется «временной жёсткостью», а оставшаяся жёсткость — «постоянной жёсткостью».
- Когда жёсткость меньше щёлочности (в мэкв/л), постоянная жёсткость отсутствует, и временная жёсткость равна общей жёсткости.
- Все природные воды ионно сбалансированы, т.е. сумма катионов в мэкв/л равна сумме анионов.
Другие ионы, обычно присутствующие в следовых количествах, но иногда не полностью незначительные, могут быть объединены с вышеуказанными:
- барий (Ba++) и стронций (Sr++) — щелочноземельные металлы и относятся к жёсткости;
- аммоний (NH4+) и калий (K+) обрабатываются как натрий;
- литий (Li+) также реагирует как натрий (Na+);
- фосфат (PO43−) относится к ЭМК;
- фторид (F−), бромид (Br−) и йодид (I−) — галогениды и ведут себя как хлорид.
Барий и стронций: растворимость сульфата бария составляет всего 2 мг/л. Ba и Sr плохо удаляются на СлКК смолах. Однако Ba (и Ra) очень хорошо удаляются на СКК смолах — настолько хорошо, что регенерация может быть затруднена.
Единицы концентрации и ёмкости
Поскольку нам нужно знать количество ионов для обмена — их масса здесь не помогает — концентрация всех этих ионов должна быть преобразована в химические «эквивалентные» единицы. Международная единица — экв·кг−1, которую мы традиционно переименовываем в эквиваленты на литр экв/л, а при низких концентрациях — мэкв/л.
| Название | Сокращение | = | мэкв/л |
|---|---|---|---|
| ppm как карбонат кальция | 1 ppm как CaCO3 | = | 0,02 |
| Французский градус | 1 °f | = | 0,2 |
| Немецкий градус жёсткости | 1 °dH | = | 0,357 |
| Гран CaCO3 на US галлон | 1 gr CaCO3/gal | = | 0,342 |
| Название | Сокращение | = | экв/л |
|---|---|---|---|
| Грамм CaCO3 на литр | 1 г CaCO3/л | = | 0,02 |
| Французский градус | 1 °f | = | 0,0002 |
| Грамм CaO на литр | г CaO/л | = | 0,0357 |
| кгр CaCO3 на куб. фут | kgr CaCO3/ft³ | = | 0,0458 |
Единицы моля следует избегать в ионном обмене, поскольку они не учитывают валентность и вносят только путаницу. Для справки: 1 экв = 1 моль / валентность.
Примеры
Таблица показывает наиболее распространённые ионы в воде и их эквивалентную массу.
| Название | Ион | г/моль | г/экв |
|---|---|---|---|
| Кальций | Ca++ | 40 | 20 |
| Магний | Mg++ | 24 | 12 |
| Натрий | Na+ | 23 | 23 |
| Калий | K+ | 39 | 39 |
| Аммоний | NH4+ | 18 | 18 |
| Хлорид | Cl− | 35,5 | 35,5 |
| Сульфат | SO4= | 96 | 48 |
| Нитрат | NO3− | 62 | 62 |
| Бикарбонат | HCO3− | 61 | 61 |
| Карбонат | CO3= | 60 | 30 |
В воде концентрации выражаются в мэкв/л. Например, если концентрация кальция составляет 90 мг/л, эквивалентная концентрация равна 90/20 = 4,5 мэкв/л.
Кремниевая кислота (SiO2), не ионизированная в обычной воде, имеет молярную массу 60. Для ионного обмена (с сильноосновной смолой в OH-форме) она считается одновалентной, поэтому эквивалентная масса также 60.
Углекислый газ (CO2) очень слабо ионизирован в обычной воде и также считается одновалентным, с молярной и эквивалентной массой 44.
Сбалансированный анализ?
Вода электрически нейтральна, даже если содержит большое количество ионов. Это означает, что число анионных зарядов точно равно числу катионных зарядов. Поэтому, после тщательного преобразования всех элементов анализа воды в единицы мэкв/л, сумма анионов должна быть равна сумме катионов.
Единственные исключения из этого правила:
- Небольшая разница из-за неточности аналитических процедур приемлема, если разница между общими катионами и общими анионами составляет менее 3%.
- При высоком pH (> 8,2), например, в присутствии аммиака, будут присутствовать гидроксидные или карбонатные ионы.
- При низком pH (скажем, < 6,8) вода может содержать либо свободную минеральную кислотность, либо свободный углекислый газ.
Пример анализа воды
Вот анализ, необходимый для расчёта установки ионного обмена (умягчение, деминерализация, декарбонизация, удаление нитратов). Это реальная вода из реки Уаза, Франция.
| Катионы | мг/л | мэкв/л | Анионы | мг/л | мэкв/л |
|---|---|---|---|---|---|
| Ca++ | 93 | 4,65 | Cl− | 67 | 1,89 |
| Mg++ | 12 | 1,00 | SO4= | 33 | 0,69 |
| Na+ | 26 | 1,13 | NO3− | 6 | 0,10 |
| K+ | 4 | 0,10 | HCO3− | 259 | 4,23 |
| Всего катионов | 6,90 | Всего анионов | 6,91 | ||
| SiO2 | 2,4 | 0,04 | |||
| pH | 7,04 | Свободный CO2 | 45 | 1,02 | |
| Электропроводность, мкСм/см | 627 | Анионная нагрузка | 7,97 | ||
| Органика (ХПК) | 2,6 | ||||
| Температура, °C | 16 | ||||
Важное примечание: Для расчёта установки ионного обмена всегда следует использовать реальный анализ воды, а не средние значения. При необходимости следует рассмотреть два или три анализа, когда солёность показывает сезонные колебания.
m- и p-Щёлочность
Щёлочность включает следующие анионы:
- Гидрокарбонат HCO3−, часто называемый бикарбонатом
- Карбонат CO3=
- Гидроксид OH−
Щёлочность в воде измеряется титрованием кислотой. Используются два разных индикатора:
- Фенолфталеин, меняющий цвет при pH 8,3, измеряет p-щёлочность
- Метиловый оранжевый, меняющий цвет при pH 4,5, измеряет m-щёлочность
Общая щёлочность — это m-Alk, и она может включать ионы OH, CO3 и HCO3. p-Alk измеряет только OH и половину ионов CO3.
HCO3− + OH− → CO3= + H2O
| Ион | = | p = 0 | p < m/2 | p = m/2 | m/2 < p < m | p = m |
|---|---|---|---|---|---|---|
| OH | = | 0 | 0 | 0 | 2p − m | p |
| CO3 | = | 0 | 2p | m = 2p | 2(m − p) | 0 |
| HCO3 | = | m | m − 2p | 0 | 0 | 0 |
Значения в таблице выражены в эквивалентных единицах, т.е. в мэкв/л, ppm CaCO3, французских или немецких градусах, не в моль/л или мг/л!
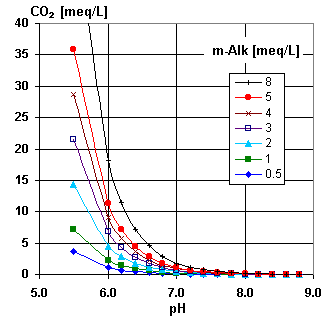
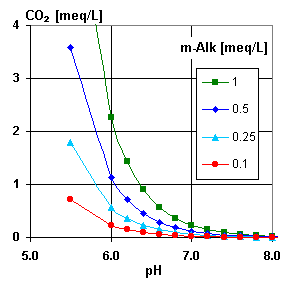
Свободный CO2 и pH
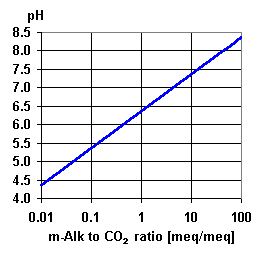
Низкое значение pH означает, что в растворе присутствуют ионы H+. В присутствии бикарбоната существует следующее равновесие:
H+ + HCO3− ⇌ H2CO3 ⇌ CO2 + H2O
Используйте график, чтобы проверить, что анализ воды, предоставленный вашим клиентом, имеет смысл, и оценить концентрацию свободного углекислого газа, если она не указана. Вы также видите, что при pH более 7,2 эта концентрация практически пренебрежима.