Основные процессы ионного обменав водоподготовке
Введение
Технология ионного обмена используется для различных задач водоподготовки:
- Умягчение (удаление жёсткости)
- Декарбонизация (удаление бикарбонатов)
- Декатионирование (удаление всех катионов)
- Обессоливание (удаление всех ионов)
- Полирование смешанным слоем
- Удаление нитратов
- Селективное удаление различных загрязнителей
Здесь вы найдёте описание вышеуказанных процессов, реакций обмена и изменений в воде. Типы смол описаны на другой странице, как и методы регенерации.
Умягчение
Природная вода содержит ионы кальция и магния, образующие малорастворимые соли. Эти катионы называются ионами жёсткости. При даже небольшом испарении воды эти катионы выпадают в осадок. Именно это вы видите, когда вода испаряется в кипящем чайнике на кухне.
Жёсткая вода образует накипь в водопроводных трубах и котлах. Сильнокислотные катиониты (СКК) в натриевой форме удаляют эти катионы жёсткости из воды.
Реакции
Вот пример с кальцием:
2 R-Na + Ca++ → R2-Ca + 2 Na+
Реакция регенерации хлоридом натрия:
R2-Ca + 2 Na+ → 2 R-Na + Ca++
Что происходит с водой
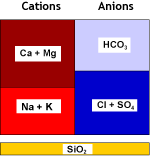
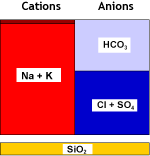
Солёность воды не изменяется, только жёсткость заменяется натрием.
Качество обработанной воды
- Прямоточная регенерация: зависит от состава воды и расхода регенеранта
- Противоточная регенерация: < 0,02 мэкв/л (1 мг/л в пересчёте на CaCO3)
Применения
- Обработка воды для котлов низкого давления
- Посудомоечные машины (умягчающий картридж)
- Пивоварни и заводы безалкогольных напитков
Декарбонизация (удаление щёлочности)
Этот особый процесс использует слабокислотный катионит. Этот тип смолы способен удалять жёсткость из воды, когда она также содержит щёлочность. После обработки вода содержит углекислый газ, который можно удалить дегазатором.
Реакции
2 R-H + Ca++(HCO3–)2 → R2-Ca + 2 H+ + 2 HCO3–
и ионы водорода соединяются с бикарбонат-анионами с образованием углекислого газа и воды:
H+ + HCO3– → CO2 + H2O
Качество обработанной воды (после дегазатора)
- Временная жёсткость: практически 0
- Общая жёсткость: = СМА (свободные минеральные анионы)
- pH: 6–7
Декатионирование
Удаление всех катионов редко практикуется само по себе, за исключением первой ступени процесса обессоливания. Используется сильнокислотный катионит (СКК) в H+-форме.
Реакции
R-H + Na+ ↔ R-Na + H+
Обессоливание (деминерализация)
Для многих применений все ионы в воде должны быть удалены. Поскольку в воде есть катионы и анионы, мы должны использовать два разных типа смол: катионит и анионит. Эта комбинированная схема даёт чистую воду. Обессоливание также называют деионизацией.
Катионит используется в водородной форме (H+), а анионит — в гидроксильной форме (OH–).
Схема СКК – (ДЕГ) – СОА
Первый этап — декатионирование:
RСКК-H + Na+ ↔ RСКК-Na + H+
На втором этапе все анионы удаляются сильноосновной смолой:
RСОА-OH + Cl– ↔ RСОА-Cl + OH–
И наконец, ионы H+ реагируют с ионами OH– с образованием воды:
H+ + OH– → H2O
Качество обработанной воды
- Электропроводность (прямоток): 5–25 мкСм/см
- Электропроводность (противоток): < 1 мкСм/см
- Остаточный кремний (прямоток): 50–200 мкг/л
- Остаточный кремний (противоток): 5–40 мкг/л
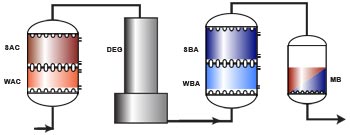
Применения
- Вода для котлов высокого давления на электростанциях
- Технологическая вода для химической, текстильной и бумажной промышленности
- Вода для аккумуляторов
- Вода для лабораторий
- Промывная вода для производства компьютерных чипов (см. Ультрачистая вода)
Полирование смешанным слоем
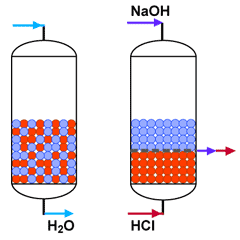
Последние следы солёности и кремния могут быть удалены на слое смолы, где смешаны высокорегенерированные сильнокислотный катионит и сильноосновный анионит.
Фильтры смешанного действия (ФСД) обеспечивают отличное качество обработанной воды, но их сложно регенерировать, так как смолы должны сначала быть разделены обратной промывкой.
Качество обработанной воды
- Электропроводность: < 0,1 мкСм/см
- Остаточный кремний: 1–10 мкг/л
- pH: не может быть измерен
Применения
- Обработка воды, предварительно обессоленной ионообменными смолами
- Полирование пермеата обратного осмоса
- Обработка турбинного конденсата
- Производство ультрачистой воды для полупроводниковой промышленности
Удаление нитратов
Нитраты могут быть селективно удалены из питьевой воды с использованием сильноосновных анионитов в хлоридном цикле, т.е. регенерируемых рассолом NaCl.
RСОА-Cl + NO3– ↔ RСОА-NO3 + Cl–
Качество обработанной воды
Зависит от состава воды, расхода регенеранта и режима регенерации. Ожидаемый проскок NO3 при противотоке: 2–10 мг/л.
Селективное удаление различных загрязнителей
Селективное удаление металлов и других загрязнителей в основном используется для питьевой воды и сточных вод. Многие из этих применений требуют специальных смол.
Примеры
- Удаление бора (борной кислоты) из питьевой воды
- Удаление перхлоратов из питьевой воды
- Удаление тяжёлых металлов из стоков: Cd, Cr, Fe, Hg, Ni, Pb, Zn
Дополнительная информация
Сокращения
- СКК: сильнокислотный катионит
- СлКК: слабокислотный катионит
- СОА: сильноосновный анионит
- СлОА: слабоосновный анионит
Ионообменные колонны
Различные типы колонн описаны на отдельной странице, как и основные принципы проектирования.
Регенерация
См. подробности о процессах регенерации.
Оригинал: © François de Dardel
Перевод: VACO Engineering, 2026