Реакции ионного обмена
Введение
На этой странице представлена общая концепция равновесия ионного обмена, коэффициенты селективности и типичные реакции различных типов ионообменных смол.
Равновесие
Когда ионообменная смола в ионной форме A контактирует с раствором, содержащим ион B, наблюдается равновесная реакция. Вот пример катионного обмена:
R-A+ + B+ ⇌ R-B+ + A+
В процессе ионного обмена ионы A будут мигрировать в раствор и замещаться ионами B из раствора до достижения равновесия. Это равновесие описывается законом действующих масс:
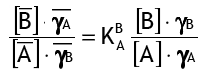 (2)
(2)где [..] обозначает концентрации, а γ — коэффициенты активности, а черта указывает на фазу смолы. K — это коэффициент селективности B+над A+ для реакции ионного обмена:
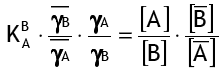 (3)
(3)В первом приближении коэффициенты активности считаются постоянными, так что упрощённый коэффициент селективности равен:
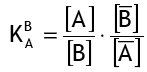 (4)
(4)Для наиболее распространённой реакции между сильнокислотной смолой в H+-форме и ионами натрия (Na+) в воде уравнение (1) принимает вид:
R-H+ + Na+ ⇌ R-Na+ + H+
А соответствующий коэффициент селективности:
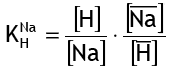 (6)
(6)Значение коэффициента K(Na/H) составляет около 1,7 для стандартной гелевой сульфокислотной сильнокислотной ионообменной смолы (см. таблицу коэффициентов селективности). Это означает, что если смола с известным составом ионов Na и H помещена в чистую воду, ионы натрия будут мигрировать в воду до тех пор, пока концентрация натрия не достигнет равновесия, определённого уравнением (6).
Для двухвалентных ионов, например (реакция умягчения):
2 R-Na+ + Ca++ ⇌ R2-Ca++ + 2 Na+
Коэффициент селективности:
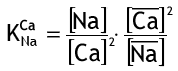 (8)
(8)Регенерация
Регенерация состоит в обращении равновесия путём увеличения концентрации иона, вытесняемого в реакции равновесия. Например, умягчитель регенерируется с использованием высокой концентрации ионов [Na+] в правой части реакции (7). Это приводит к смещению реакции влево.
Работа колонны
В нормальной практике ионного обмена смола не остаётся в равновесии с раствором. Вместо этого раствор отводится на выходе из колонны, так что равновесие постоянно смещается вправо. Посмотрим снова на уравнение (1):
R-A+ + B+ ⇌ R-B+ + A+
Обработанный раствор — обогащённый ионами A+ и обеднённый ионами B+ — уносится и замещается необработанным раствором, в котором концентрация ионов A+низкая, а [B+] высокая. Это позволяет смоле удалять больше ионов B+из раствора, поскольку равновесие смещается вправо.
Рассмотрим теперь специфическое поведение распространённых ионообменных смол.
Сильнокислотные смолы (СКК)
Когда смола изначально находится в водородной форме H+(R-SO3−H+, сокращённо R-H), она может удалять все катионы из раствора:
R-H + Na+Cl− → R-Na + H+Cl−
Второй пример с бикарбонатом кальция:
2 R-H + Ca++(HCO3−)2 → R2-Ca + 2 H2CO3
Здесь реакция является нейтрализацией, так как бикарбонатный анион щелочной. Она необратима, поскольку нельзя регенерировать СКК смолу угольной кислотой.
Реакции (9) и (10) типичны для первой стадии деминерализации. См. декатионирование.
Когда смола изначально находится в натриевой форме Na+, СКК смолы удаляют двухвалентные катионы из воды, но не другие одновалентные катионы, поскольку разница селективности с K+ или NH4+ слишком мала.
2 R-Na + Ca++(HCO3−)2 → R2-Ca + 2 Na+HCO3−
Эта реакция умягчения обратима, но регенерацию не проводят бикарбонатом натрия из-за риска осаждения карбоната кальция. Вместо этого используют хлорид натрия.
Слабокислотные смолы (СлКК)
Эти смолы реагируют иначе, так как они лишь слабо ионизированы в регенерированной (H+) форме. С нейтральными солями реакции не наблюдается:
R-COOH + Na+Cl− ← ничего
Объяснение: если бы реакция произошла, она создала бы HCl как продукт. Но поскольку смола является более слабой кислотой, чем продукт соляной кислоты, смола немедленно вернётся в кислотную форму.
Для того чтобы слабокислотная смола прореагировала, она должна быть диссоциирована. Следовательно, ион H+ в кислоте должен быть удалён щёлочью. Например, следующая реакция немедленная и необратимая:
R-COOH + Na+OH− → R-COO−Na+ + H2O
Это реакция нейтрализации, в которой продуктом является вода (отсюда необратимость).
В следующей реакции:
2 R-COOH + Ca++(HCO3−)2 → (R-COO−)2Ca++ + 2 H2CO3
бикарбонатный ион «отрывает» H от карбоксильной группы, так что она становится ионизированной. Слабокислотные катионитные смолы используются в водоподготовке для удаления бикарбонатной жёсткости из воды. Это процесс декарбонизации. См. комплекс на странице структуры смол.
С бикарбонатом натрия вместо бикарбоната кальция или магния реакция также происходит, но СлКК смола имеет гораздо меньшее сродство к одновалентным ионам, поэтому рабочая ёмкость низкая:
R-COOH + Na+HCO3− → R-COO−Na+ + H2CO3
После преобразования в Na+-форму двухвалентные ионы могут обмениваться даже в отсутствие щелочных анионов:
2 R-COO−Na+ + Ca++Cl−2 → (R-COO−)2Ca++ + 2 Na+Cl−
Умягчение на СлКК смоле очень эффективно благодаря высокой селективности этих смол к ионам жёсткости. Остаточная жёсткость в обработанной воде очень низкая, поэтому процесс, описываемый реакцией (16), используется для умягчения воды в присутствии высокой концентрации натрия. На практике СлКК смолу преобразуют в Na+-форму с помощью кальцинированной соды (Na2CO3) или едкого натра (NaOH) перед использованием для умягчения.
Выводы: при нормальном использовании (H-цикл, регенерация HCl) СлКК смола удаляет только жёсткость, и только при наличии щёлочности; для умягчения (Na-цикл) СлКК смолу сначала необходимо преобразовать в Na-форму с помощью щёлочи.
Сильноосновные смолы (СОА)
Когда смола изначально находится в гидроксидной форме OH−(R-CH2-N(CH3)3+OH−, сокращённо R-OH), она может удалять все анионы из раствора:
R-OH + Na+Cl− → R-Cl + Na+OH−
Регенерация СОА смол осуществляется обращением реакции (17) с помощью относительно концентрированного раствора едкого натра.
После катионного обмена [реакция (9)] реакция имеет вид:
R-OH + H+Cl− → R-Cl + H2O
Это реакция нейтрализации сильной кислоты, в которой продуктом является вода. Следовательно, она необратима.
СОА смола в OH−-форме также обменивает слабые кислоты, такие как угольная:
R-OH + H2CO3 → R-HCO3 + H2O
Вторая реакция происходит, пока на смоле есть ионы OH−:
R-HCO3 + R-OH → R2-CO3 + H2O
Карбонатные ионы располагаются на двух функциональных группах смолы. Обратите внимание, что на практике OH−-формные смолы не используются для удаления бикарбоната или карбоната из нейтральной воды, если она содержит жёсткость, из-за опасности осаждения гидроксида или карбоната кальция.
Смола также реагирует с очень слабыми кислотами, такими как кремниевая (SiO2) или борная (H3BO3). В следующей реакции кремниевая кислота представлена как H2SiO3:
R-OH + H2SiO3 → R-HSiO3 + H2O
Когда СОА смола изначально находится в хлоридной форме Cl−, она может обменивать любые анионы, к которым имеет более высокую селективность(см. таблицу селективности):
R-Cl + NO3− ⇌ R-NO3 + Cl−
Реакция (22) представляет процесс удаления нитратов, для которого используются специальные СОА смолы с различными функциональными группами с повышенной селективностью к нитратам.
Слабоосновные смолы (СлОА)
Наиболее распространённая функциональная группа — R-CH2-N(CH3)2. Эти смолы не ионизированы в регенерированной форме свободного основания. Поэтому они не реагируют с нейтральными солями:
R-CH2-N(CH3)2 + Na+Cl− ← ничего
Для того чтобы СлОА смолы прореагировали, они должны быть сначала ионизированы. Только сильная кислота может протонировать амин, который превращается в четвертичный аммоний. Во многих случаях реакция происходит после декатионирования воды или обрабатываемого раствора (9):
R-CH2-N(CH3)2 + H+Cl− → R-CH2-NH+(CH3)2Cl−
Поглощение всего соединения соляной кислоты превращает СлОА смолу в её солянокислую (.HCl) форму. Аналогичные реакции происходят с сульфатом и нитратом после катионного обмена.
Однако щёлочность СлОА смолы недостаточно сильна для протонирования активной группы слабыми кислотами, поэтому эти смолы не могут удалять кремниевую кислоту или углекислый газ из воды:
R-CH2-N(CH3)2 + H2CO3 ← ничего
Слабоосновные смолы используются для удаления только сильных кислот, но они имеют более высокую ёмкость и легче регенерируются, чем СОА смолы.
Хелатирующие смолы
Эти смолы с несколькими различными функциональными группами (см. примеры селективных типов смол) способны образовывать комплексы с металлами. См. также пример комплекса на странице структуры смол.
Дополнительная информация
- Селективность (общая информация)
- Таблицы селективности для катионообменных и анионообменных смол
- Процессы водоподготовки для практического применения вышеуказанных реакций
- Применения ионного обмена (водоподготовка и многие другие области)
- Различные типы смол с примерами
- Структура ионообменных смол в общем
- Таблица Менделеева с информацией об удалении различных ионов смолами